La respiration : le rôle des barorécepteurs dans le contrôle de la ventilation
 Comme le montrent les quelques expériences que nous avons décrites jusque-là, l’expérimentation animale était largement pratiquée en Europe au début du XIXe siècle. Ce fut en particulier le cas au Collège de France, où la chaire de physiologie était détenue par François Magendie (1785-1855). L’éminent physiologiste fit, en marge de ses recherches sur le fonctionnement du système nerveux, quelques observations sur l’influence des mouvements respiratoires sur le «cours du sang dans les artères». A la fin des années 1820, avec la mise au point, par le physiologiste Jean-Léonard-Marie Poiseuille (1799-1869), d’un hémodynamomètre à mercure permettant de mesurer précisément la pression artérielle, les relations entre ce dernier paramètre et les mouvements respiratoires purent être rigoureusement étudiées.
Comme le montrent les quelques expériences que nous avons décrites jusque-là, l’expérimentation animale était largement pratiquée en Europe au début du XIXe siècle. Ce fut en particulier le cas au Collège de France, où la chaire de physiologie était détenue par François Magendie (1785-1855). L’éminent physiologiste fit, en marge de ses recherches sur le fonctionnement du système nerveux, quelques observations sur l’influence des mouvements respiratoires sur le «cours du sang dans les artères». A la fin des années 1820, avec la mise au point, par le physiologiste Jean-Léonard-Marie Poiseuille (1799-1869), d’un hémodynamomètre à mercure permettant de mesurer précisément la pression artérielle, les relations entre ce dernier paramètre et les mouvements respiratoires purent être rigoureusement étudiées.
L’expérience de Poiseuille (1828):
L’hémodynamomètre à mercure de Poiseuille est constitué d’une canule que Poiseuille introduit dans différentes artères d’un chien vigil : carotide, axillaire, humérale, crurale et fémorale reliée à un tube en U gradué et rempli de mercure. Dans chaque artère où il mesure, grâce à ce dispositif, la pression sanguine, Poiseuille note que l’inspiration s’accompagne d’un abaissement de la colonne de mercure alors qu’un effet inverse est associé à chaque expiration :
«De ces dernières remarques, nous concluons que l’influence des mouvements respiratoires sur le cours du sang artériel est augmentée dans les grosses comme dans les petites artères, lorsque de violents efforts respiratoires succèdent à des respirations ordinaires; mais que cette influence, spécialement dans les grosses artères, est telle que, dans les inspirations, la force qui meut le sang est très près d’être nulle, si elle ne l’est pas ; et qu’en revanche, dans les expirations correspondantes cette force devient presque deux fois plus grande que dans l’état normal. […] Si ces développements ne dépassaient pas déjà les bornes que nous nous étions prescrites, nous rappellerions que c’est en effet dans les efforts de toux, dans les exclamations de la colère […] que l’aorte, que les tumeurs anévrysmales se rompent, que surviennent les hémorragies nasales, cérébrales […], nous parlerions surtout du soin qu’il faut avoir quand on explore le pouls, de bien s’assurer si la respiration se fait régulièrement ; car si à de certains intervalles, par suite d’émotions vives, le malade fait une profonde inspiration, une pulsation pourra se faire attendre, être nulle, d’où l’on conclura à tort que le pouls est irrégulier ou même intermittent […].»
Dans son travail de thèse, Poiseuille a mis en évidence, sans les comprendre, les conséquences d’une modification de la pression intrathora- cique sur la pression artérielle. Une augmentation de la pression intrathoracique, lors d’une expiration forcée par exemple, augmente par un effet mécanique le volume d’éjection systolique, c’est-à-dire le volume de sang éjecté du cœur lors de la contraction ventriculaire gauche. Comme la pression artérielle dépend du volume d’éjection systolique, on comprend l’influence hypertensive de l’expiration.
L’expérience de Heymans (1930):
La nature des mécanismes qui relient pression artérielle et ventilation est étudiée en 1930 par le médecin et pharmacologue belge Cornélius Jean-François Heymans (1892-1968). Il s’inspire pour cela de la technique des circulations céphaliques croisées mise au point au tournant du XIXe siècle par son compatriote Léon Frédéricq.
Heymans réalise une préparation de tête isolée chez un premier chien (chien B) : outre la trachée et la moelle épinière, les seuls liens entre la tête et le tronc de ce dernier sont représentés par les deux nerfs pneumogastriques, dont le rôle dans le contrôle de la ventilation pulmonaire est établi depuis la fin du XIXe siècle. Cette tête isolée est perfusée par le sang issu du tronc d’un chien donneur (chien A).
Il injecte de l’adrénaline dans le tronc du chien B afin d’y provoquer une augmentation de pression artérielle. Il observe, chez le chien B, une diminution de la ventilation allant jusqu’à l’apnée. Puisque les seuls liens entre tête – où, comme on le sait déjà, les centres respiratoires bulbaires contrôlent la ventilation pulmonaire – et tronc de ce chien sont les deux nerfs pneumogastriques, Heymans montre ainsi que le phénomène observé a pour origine un mécanisme réflexe de nature nerveuse impliquant ce nerf. En outre, l’hypertension n’affectant pas la tête, puisqu’elle est irriguée par le sang du chien A, elle est nécessairement détectée par des récepteurs périphériques. Heymans conclue donc que le centre respiratoire du bulbe rachidien de la tête isolée B a été inhibé par l’augmentation de pression artérielle périphérique et que l’apnée du chien B a pour origine une hypertension qui a été détectée, au niveau vasculaire, par des barorécepteurs reliés à ce centre nerveux par des fibres vagales.
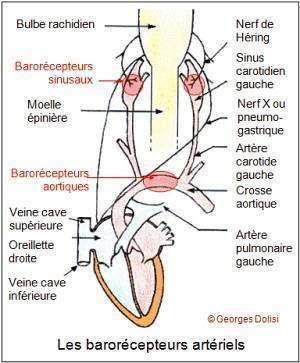
Peu avant cette expérience, dans les années 1920, Heymans et ses collaborateurs ont localisé ces capteurs périphériques de la pression artérielle au niveau des sinus carotidiens et de la crosse aortique. Heymans va montrer expérimentalement l’implication de ces derniers dans le contrôle de la ventilation. En effet, en clampant les carotides d’un chien en amont des barorécepteurs, ce qui provoque une hypotension au niveau de ceux-ci, il induit une hyperpnée (forte augmentation de la fréquence et de l’amplitude des mouvements ventilatoires) chez l’animal. La mise enjeu des barorécepteurs du sinus carotidiens a donc provoqué une hyperventilation. Heymans confirme par cette expérience que ces mêmes barorécepteurs sont également impliqués dans une boucle de régulation de la pression artérielle tendant à assurer la constance de ce paramètre du milieu intérieur: l’hypotension carotidienne induit en retour une hypertension généralisée.
Notons que de 1927 à 1939, Heymans caractérisera le fonctionnement d’autres récepteurs aortiques et carotidiens: les chémorécepteurs et leur implication dans le contrôle de la ventilation. Il étudiera par ailleurs les effets de l’hypercapnie – qui se traduit par une augmentation d’acidité sanguine – et de l’hypoxie – carence en dioxygène — sur la ventilation. Les travaux de Heymans sont récompensés par l’attribution du prix Nobel de médecine et de physiologie en 1938.